

近年来,多种小分子新药发现技术的爆发为生物医药创新激发了新的生命力。FBDD(基于片段的药物发现)作为当今主流的药物发现技术,为新药研发带来哪些可能性?6月28日,维亚生物“FIC新药发现突围之路—FBDD策略篇”沙龙同步线上线下成功举办,携手业界先锋、学术界专家等,从更大视野、更多维度探讨FBDD在药物发现中的前沿技术与洞见,以共同推动生物医药研发实现新的跨越。下面整理了各位嘉宾的部分精彩观点以饕读者。错过本期直播的伙伴,可点击此处观看,或者关注“维亚生物”视频号了解本期完整版视频回放。
变局时代,FBDD驱动创新药新机遇
维亚生物首席创新官兼创新中心负责人戴晗博士

小分子药物在医药市场中一直占据着主要地位,虽然近年来抗体/蛋白药物和CGT的出现对小分子药物产生一定的市场竞争,但随着创新技术的不断涌现,小分子新药研发又萌发了新的生机。戴晗博士由此引出新型小分子筛选技术平台——基于片段的药物发现FBDD,他指出,与传统高通量筛选HTS相比,片段化合物分子量更小,苗头化合物更有潜力,有更多的结构优化空间,且片段化合物和蛋白结合位点契合度更高,更可能产生高结合效率的先导化合物。随后,他分别以MAT2A、Bcl-2靶点为例介绍了FBDD常用优化策略——片段扩展法和片段连接法。
谈到FBDD技术,当然也少不了它使用的筛选方法,尤其是亲和力筛选。戴晗博士讲述了维亚的亲和力筛选平台如何在非共价结合/共价结合化合物筛选中发挥作用,并进一步分享了ASMS、晶体浸泡、SPR、Intact-MS、TSA等在各自使用场景中的应用。找到片段苗头分子后,一般要解析出其共晶结构,截至2022年底,维亚累计向客户交付超过48925例蛋白结构,其中2022年新增交付约14534例蛋白结构,研究累计超过1878个独立药物靶标,其中2022年新增交付68个。最后,戴晗博士列举小分子PCSK9变构抑制剂和新机理首创抗癌药发现案例进一步阐述了维亚新药发现技术平台的应用。
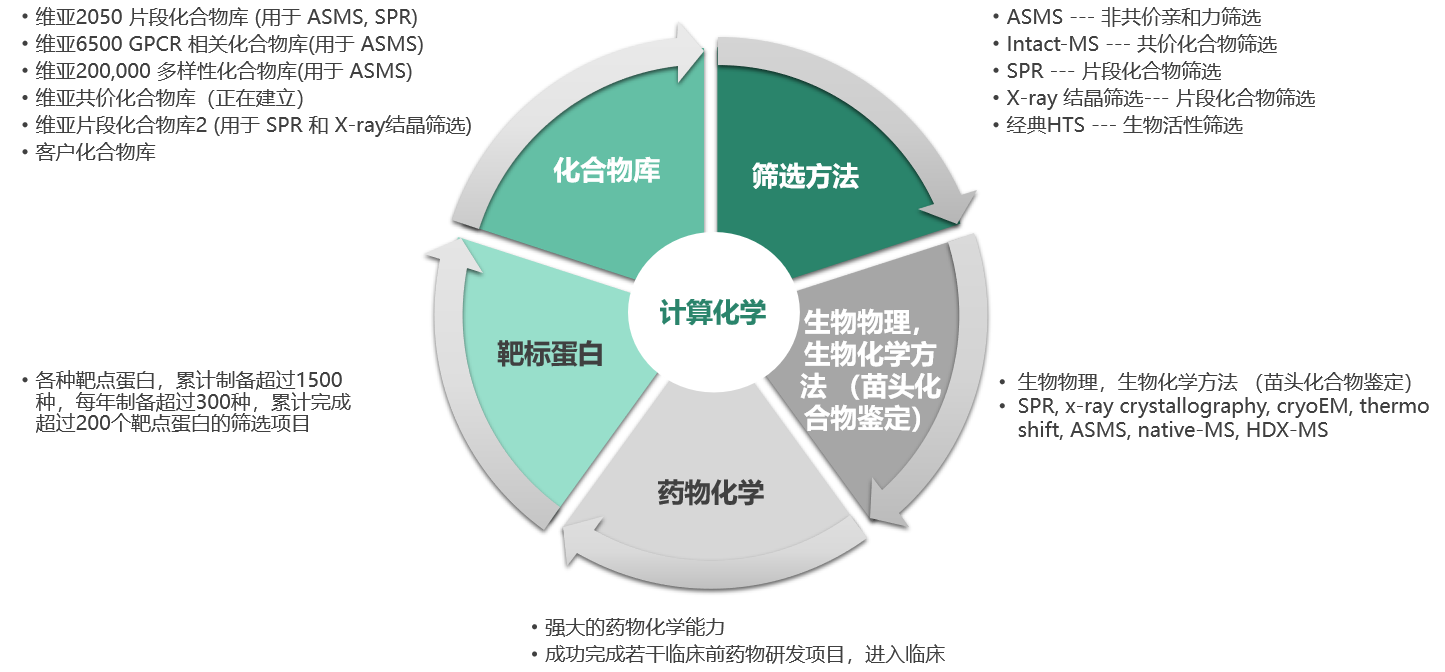
(维亚新药发现技术平台)
同步辐射光源在FBDD开发策略的应用
中国科学院上海高等研究院研究员汪启胜博士

都知道,同步辐射光源的出现,使得X射线晶体衍射技术得到了极大的发展。汪启胜博士在演讲中介绍了上海同步辐射光源(简称“SSRF”)线站的布局,目前约有40条开放的线站,包括了首条晶体学线站BL17U1、BL17U1搬迁线站(BL02U1)、P2生物防护蛋白质晶体学线站(BL10U2)、高性能膜蛋白晶体学线站(BL17UM)及微束白光劳厄衍射线站(BL03HB)。同时他还介绍了晶体学线站高通量实验技术,SSRF使用新型探测器,保证晶体衍射数据的高效率和高质量,对比2016年和2017年的变化,理想状态下,采集时间从30min迭代到30s,数据从4867套增长至10096套。另外,他还分享了SSRF目前正在搭建中的FBDD实验平台。
基于片段药物发现策略的蛋白翻译后修饰体系新药研究
中国科学院上海药物研究所研究员、博士生导师熊兵博士

如何开发药物治疗疾病?一直与人体的奥秘息息相关。人类复杂性的来源,更多地在于基因如何使用,而不是基因的数目,在于蛋白质中发生的成千上万的化学变化,或者在于通过基因组非编码区控制这些蛋白质的生产。基于此,熊兵博士首先诠释了他选择蛋白翻译后修饰体系作为靶点的原因。然后,他又从药物开发的角度对FBDD方法的优势进行了分析。与高通量筛选方法相比,片段分子库具有多样性高、库容量小等特点,虽然存在活性低的不足但是其配体效率更高。目前,FBDD的应用大致分为两类:一类是基于常规片段库进行药物发现;一类是基于共价片段库进行靶点发现。另外,使用FBDD方法,还可以考察靶点的可靶向性、发现多种结合位点及结合PROTAC策略设计蛋白降解剂等。其次,根据JMC最新统计数据,2018-2021年期间,在所有药物筛选方法中,有7%的临床新分子是从片段筛选获得的,且占比呈上升的态势。此外,从FBDD的理性基础角度出发,他认为,基于片段的药物发现,是一种新的思考模式,是一种减法思维。
在此,熊兵博士也介绍了他所在课题组所建立的FBDD技术平台,现有片段库约有2000个分子,筛选方法完善,具有多个靶点的研发经验。随后,他还列举多个案例阐述了FBDD在翻译后修饰靶点方面的研究。在Ras脂化-转运蛋白PDEδ的抑制剂研究中,他们课题组通过FBDD技术成功研发了全新的结构类型,最好的化合物达到26 nM,活性提高2000倍。
最后他特别强调,FBDD研发策略,离不开复合物晶体结构的支撑及后期深入的化学结构改造,同时分别举例说明了从Fragment出发应用片段连接(Fragment link),片段生长(Fragment growth)及片段合并(Fragment merge)等策略快速的提高化合物活性的实际应用。并指出作为一种高效经济的活性分子药物方法,FBDD在发现新结合位点(正构、变构位点)、结合PROTAC/RiboTAC技术进行药物开发等方面大有可为。
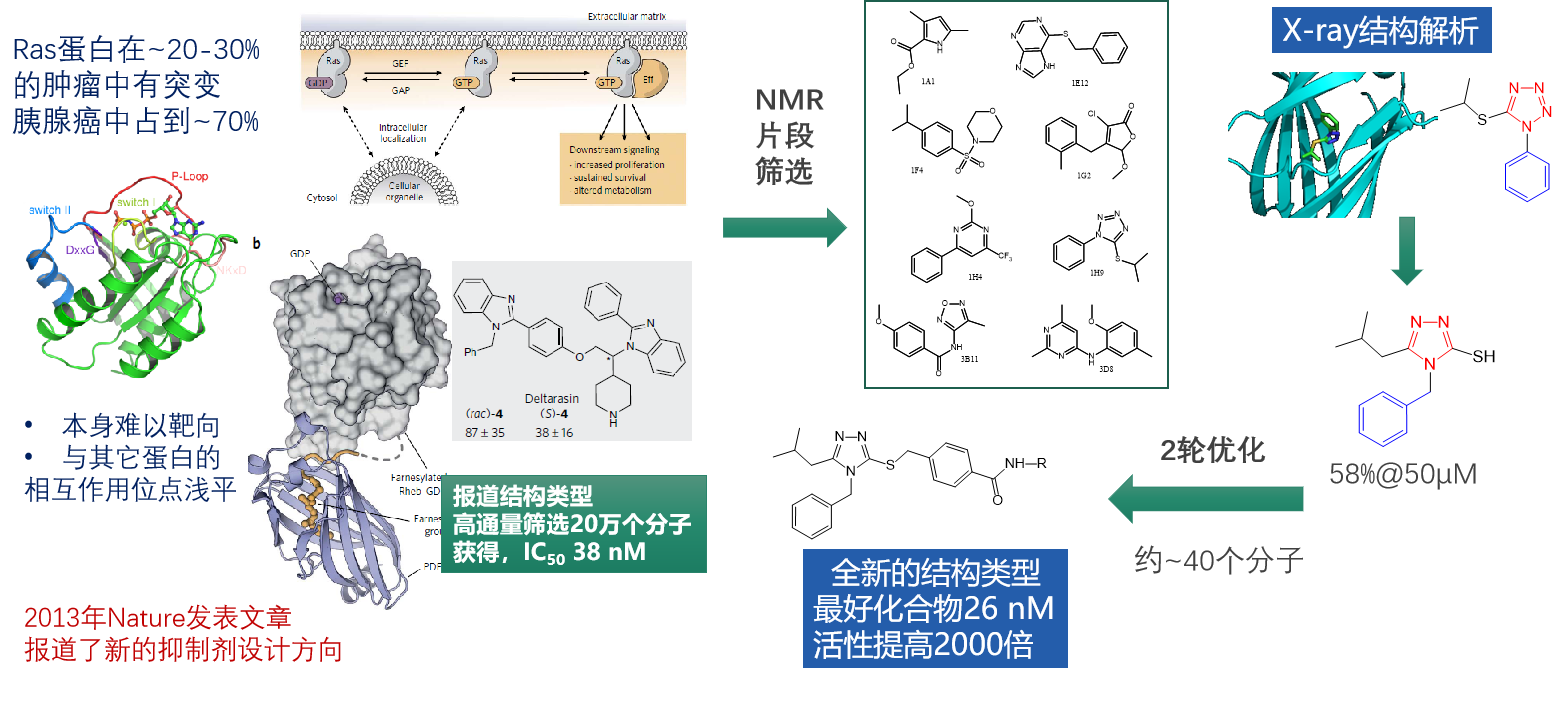
(案例:Ras脂化-转运蛋白PDEδ的抑制剂研究)
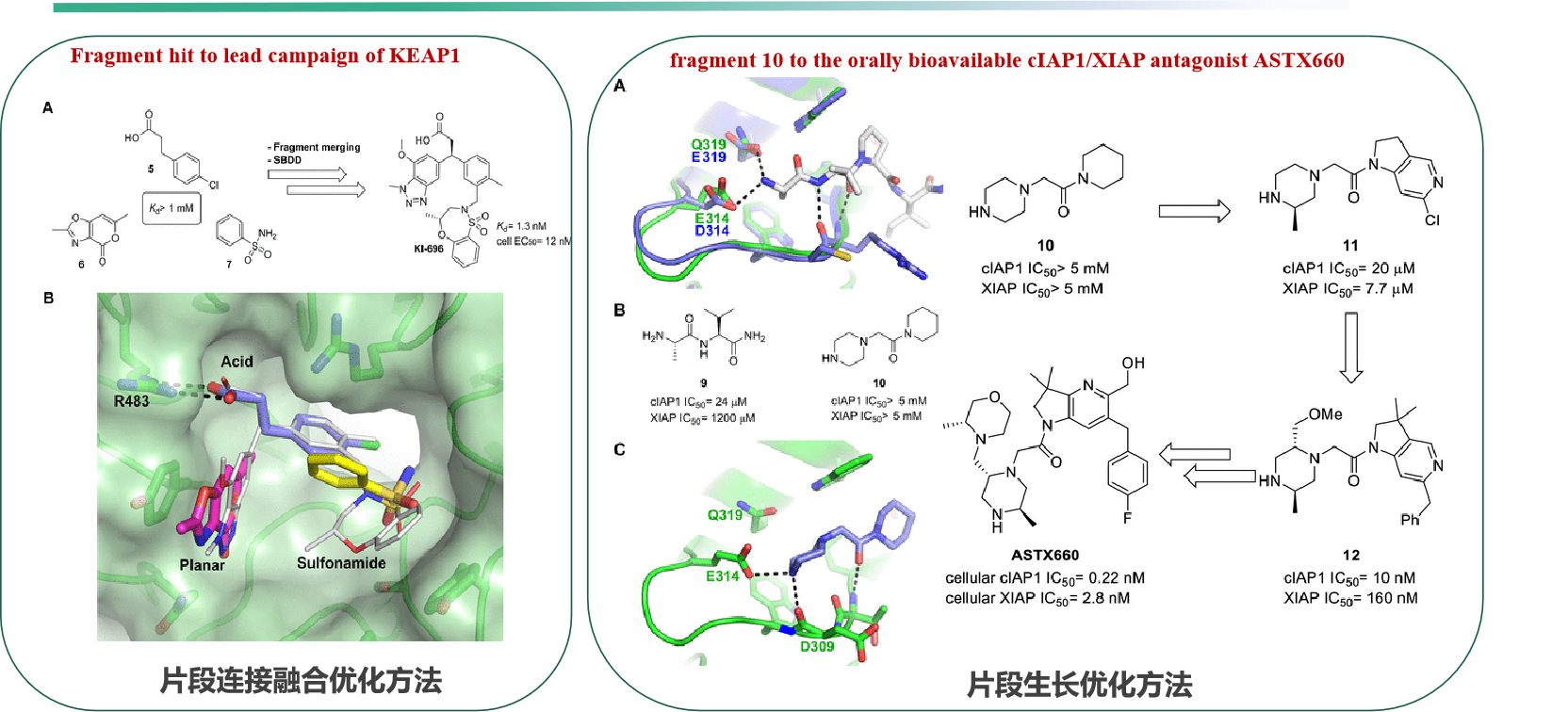
(案例:E3连接酶的抑制剂研究)
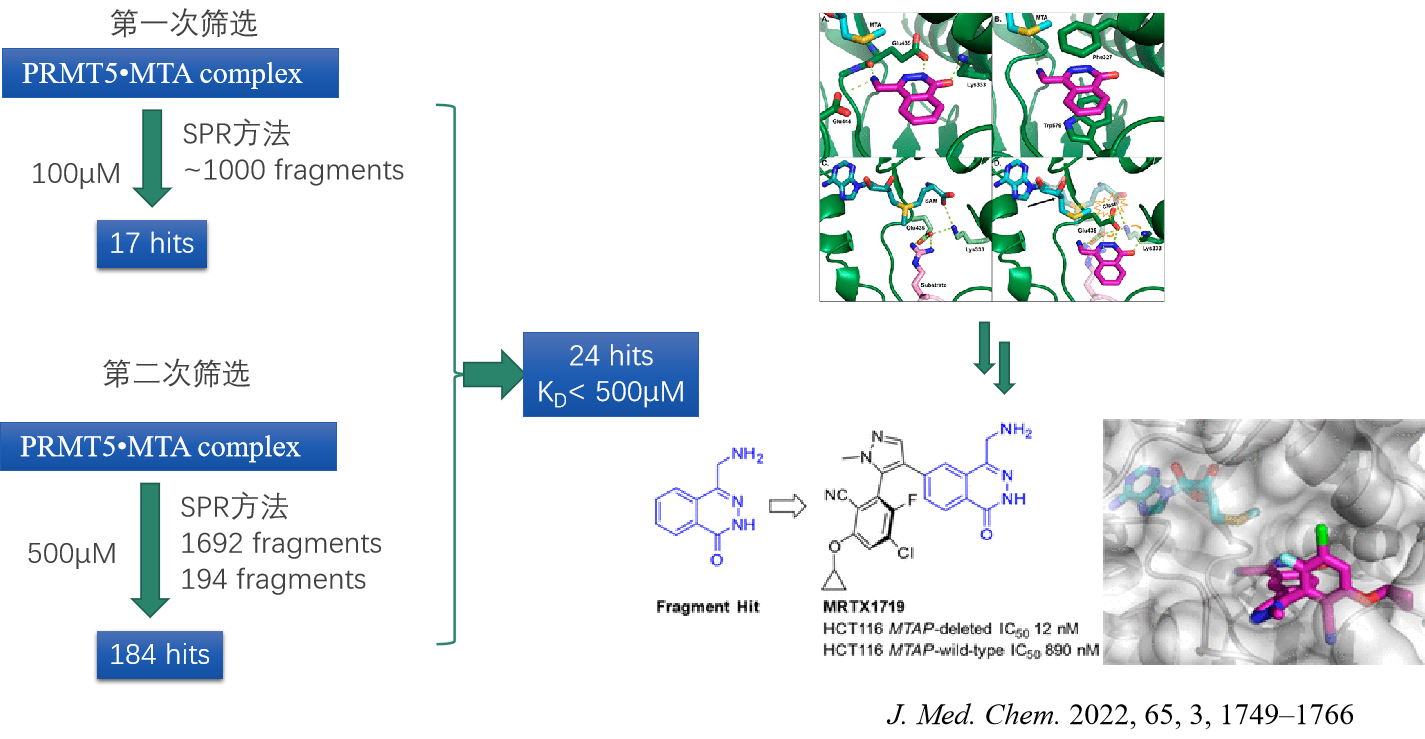
(案例:PRMT5抑制剂-MRTX1719)
圆桌讨论
探索药物发现——药物筛选方法与成功案例

(从左往右:中国科学院上海药物研究所研究员、博士生导师许叶春博士、维亚生物首席科学官叶志雄博士、特科罗创始人、董事长兼总经理王增全博士、科因生物创始人、首席执行官王一恺博士、中国科学院上海药物研究所研究员、博士生导师熊兵博士)
在叶志雄博士的主持下,熊兵博士、许叶春博士、王一恺博士、王增全博士共同探讨了以下4个议题。
Q1
近年来有6个FDA获批的药物和50多个临床化合物的研发是从FBDD开始的。各位嘉宾能对FBDD技术可以运用在什么样的靶点上,目前有什么常用到筛选方法和化合物库简单地聊一下?
王增全博士:从产业角度出发,如何在最短的时间里找到苗头化合物,并真正将其推进至临床,是至关重要的。对于小公司来说,没办法筛选很大规模的化合物库,而FBDD在这方面优势明显,它的片段库化合物可以是几百个、几千个甚至上万个,没有局限性。另外,技术层面上,像膜蛋白这类难成药的靶点应用FBDD还是比较具有挑战性的,首先这类靶点的蛋白制备就存在很大的难度,然后如何运用到片段化合物的筛选中,找到苗头化合物,及验证其是否为真正的苗头化合物,这一过程需要投入大量的时间。所以从产业的角度考虑,企业在选择某种技术时,需要仔细、综合的考虑靶点的选择、库的选择等多个因素。
熊兵博士:有研究表明,增加SP3杂化碳的数目,可使得化合物库更加立体,对复杂靶点有更高的获得活性片段的概率。针对GPCR靶点,他认为随着冷冻电镜技术的发展,FBDD在该领域的应用也会越来越广泛。
Q2
FBDD与其他筛选方法相比,有哪些优势与局限性?FBDD后续需要大量的优化工作,有什么药物研发技术能对优化工作有所帮助?
许叶春博士:每一种筛选方法都有其优缺点和使用范围,具体情况要具体分析。就FBDD而言,它涉及到各种筛选方法的使用,不需要局限于哪一种。但需要特别注意的是,相比HTS、DEL等,FBDD筛选出的苗头化合物的亲和力会相对弱一些,因此,需要重点关注如何筛选发现弱结合片段,尤其是针对大家都有提到的GPCR等靶点,没办法使用经典的酶活方法来进行筛选。在这一情况下,可以考虑发展多个assay,比如SPR、质谱、TSA等,相互交叉验证。此外,她还强调,开展FBDD项目时,如果片段结合模式不清楚,这对于后续结构优化无异于盲人摸象。所以在有条件的情况下,选择基于晶体的FBDD筛选不失为一个好的策略。
王增全博士:FBDD的一大挑战在于其较高的假阳性。过去FBDD研究的靶点一般较为容易,但对于比较难成药的靶点,FBDD面临的挑战更大。像如今使用FBDD方法获批上市的6款药物,都属于激酶。激酶具有很好的结合位点,也易于找到苗头化合物。与此同时,FBDD也有着不可否认的独特性,除了发现活性中心抑制剂,还可以用来找到别构抑制剂,这是传统筛选方法难以做到的。所以,在应用某项技术进行药物研发时,务必要考虑靶点、筛选方法及后续进程的开展。此外,他强调道,晶体结构在FBDD中发挥了关键作用。
Q3
FBDD也为难成药靶点的药物开发带来了希望。各位觉得FBDD在难成药靶点的应用上目前处于一个怎样的水平?会成为难成药靶点蛋白或者非蛋白靶点的理想筛选方法吗?比如说近年来火热的PROTAC和RNA靶点。
熊兵博士:对于难成药靶点,他认为FBDD与PROTAC技术是一个天然的、很好的结合。片段分子量较小,既使与linker或者E3连接酶连接上,分子量依然在可控范围内。对于这种分子的优化,其PK难度相对较小。反之,如果是复杂的分子与linker、E3连接酶相加,会使得分子量过大。之前有做过研究,在临床前小动物PK阶段是不错的,但是到了大动物PK参数就变化很大。因此在人体内PK很难预料,存在很大的风险。他表示,采用FBDD策略能很好地控制分子量,有助于保证PK一致性。
Q4
随着AI技术的发展,药物研发行业对AI技术也有非常高的关注和投入。在到具体应用层面上,各位嘉宾觉得AIDD/CADD与FBDD如何协同应用?未来发展趋势如何?
王一恺博士:首先,他认为无论是AIDD还是CADD,它们都是在算力普惠可及的前提下,基于某种方程的求解或者拟合。然后就与FBDD的协同应用上,他体会比较深的一件事是,科因生物从2020年开始搭建基于片段的计算平台,与专家经验相比,计算机的独特优势在于其可以大规模、高效探索所有可能的化学空间,并找出最有可能与蛋白相结合的分子。他还透露,科因生物目前已经具备基于片段的湿实验筛选验证能力,以片段和蛋白共晶中埋藏的氢键为计算起点,将极大提升分子设计准确度和优化迭代效率。这样的结合将会使FBDD成为更有效的药物发现工具。
Copyright © 维亚生物 All Rights Reserved. 沪ICP备19036061号